El Vikipedio, la libera enciklopedio
| Kalia per-reniato
|

|
| Plata kemia strukturo de la Kalia per-reniato
|
  
|
| Tridimensia kemia strukturo de la Kalia per-reniato
|
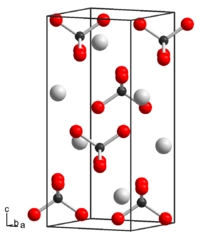
|
| Kristala strukturo de Kalia per-reniato
|
| Alternativa(j) nomo(j)
|
|
|
| Kemia formulo |
KReO4
|
| CAS-numero-kodo |
10466-65-6
|
| ChemSpider kodo |
2894851
|
| PubChem-kodo |
3661560
|
| Fizikaj proprecoj
|
| Aspekto |
blanka pulvoro
|
| Molmaso |
289301 g·mol−1
|
| Denseco |
4.887g cm−3[1]
|
| Fandpunkto |
555 °C
|
| Bolpunkto |
1370 °C
|
| Refrakta indico |
 1,643 1,643
|
| Solvebleco |
Akvo:11,9 g/L
|
| Mortiga dozo (LD50) |
692 mg/kg (buŝe)
|
| Sekurecaj Indikoj
|
| Riskoj |
R8 R22 R36/37/38 R50 R53
|
| Sekureco |
S17 S26 S27 S36/37/39
|
| Pridanĝeraj indikoj
|
| Danĝero
|
| GHS Damaĝo Piktogramo |
|
| GHS Signalvorto |
Averto
|
| GHS Deklaroj pri damaĝoj |
H272, H315, H319, H335
|
| GHS Deklaroj pri antaŭgardoj |
P210, P220, P221, P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P370+378, P403+233, P405, P501[2]
|
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo
(25 °C kaj 100 kPa)
|
Kalia per-reniato aŭ K2ReO4 estas neorganika kombinaĵo, salo de alkala metalo kaj reniata acido, senkoloraj aŭ blankaj kristaloj iomete solveblaj en akvo kaj etanolo. Ĝia kristala strukturo estas kvaredra kaj ĝi estas potenca oksidiganto. Ĝi estas uzata en spektrometrio kaj en laboratorio kiel kemia reakcianto. En farmakologio ĝi uzatas en la sintezo de la teknecio kaj renia organometala radiofarmaciaĵoj.
- Preparado de per-reniato de kalio per dissolvado de la renia oksido en solvaĵo de kalia hidroksido:
|

|
|

|
|

|
- Kalia per-reniato fandiĝas kun alkaloj, estigante perokso-reniatojn[3]:
|

|
- La renia elemento estiĝas per rekta reduktado kun hidrogeno, unue ĉe 520 °C, kaj poste ĉe 1000 °C[4]:
|

|
- Kalia per-reniato reakcias kun sulfida acido en ĉeesto de forta acido:
|

|
|

|
| Neorganikaj saloj de kalio |
|---|
 | |
|










