에스테르
Ester에스테르란 카르본산 및 알코올의 치환 반응과 같이 적어도 1개의 –OH 하이드록실기가 –O-알킬기(알콕시)[1]로 치환된 옥소산(유기 또는 무기)에서 유래한 화합물이다.글리세리드는 글리세롤의 지방산 에스테르입니다; 그것들은 지질 주요 종류 중 하나이고 동물성 지방과 식물성 기름의 대부분을 포함합니다.
에스테르는 전형적으로 좋은 냄새를 가지고 있다; 낮은 분자량의 것은 일반적으로 향기로 사용되며 에센셜 오일과 페로몬에서 발견된다.이들은 광범위한 플라스틱, 가소제, 수지 [2]및 래커의 고급 용매 역할을 하며, 상업용 [3]시장에서 가장 큰 규모의 합성 윤활제 중 하나입니다.폴리에스테르는 중요한 플라스틱으로, 에스테르 조각으로 연결된 모노머를 가지고 있습니다.포스포에스터는 DNA 분자의 골격을 형성한다.니트로글리세린과 같은 질산에스테르들은 폭발성으로 알려져 있다.
명명법
어원학
에스테르라는 단어는 1848년 독일의 화학자 레오폴드 그멜린에 [4]의해 만들어졌는데, 아마도 독일의 에시게테르(Essigéther, "초산 에테르")의 축약어일 것이다.
IUPAC 명명법
에스테르 이름은 모 알코올과 모산(모산은 유기 또는 무기)에서 유래했습니다.가장 단순한 카르본산으로부터 유래한 에스테르는 일반적으로 IUPAC 명명법 메타노에이트, 에탄올에이트, 프로판올에이트 및 부탄올에이트와 같은 전통적인 "삼원적 이름"에 따라 명명된다.반면, 보다 복잡한 카르본산으로부터 유도된 에스테르들은 산 이름 뒤에 -oate 접미사가 이어지는 체계적 IUPAC 이름을 사용하여 더 자주 명명된다.예를 들어 헥실카프릴레이트라고도 하는 에스테르헥실옥탄산염은 CH(CH2)6CO23(CH2)5CH라는 식이다3.
유기 에스테르의 화학식은 보통 RCOR,의2 형태를 취하며, 여기서 R are은 각각 카르본산과 알코올의 탄화수소 부분이다.예를 들어 부탄올과 아세트산(에탄올)에서 유래한 아세트산 부틸(에탄올)과 아세트산(에탄올)은3249 CHCOCH로 표기된다.BuOAc와 CHCOOCH를349 포함한 대체 제시가 일반적이다.
고리형 에스터는 유기산 또는 무기산으로부터 파생된 것이든 상관없이 락톤이라고 불립니다.유기락톤의 예로는 γ-발레로락톤이 있다.
정형외과 의사
유기 에스테르 중 흔치 않은 부류는 RC(3OR′)라는 공식의 정형외과이다.트리에틸로토포름산(HC(OCH25))3은 오르토포름산(HC(OH))3과 에탄올에서 그 이름(그러나 합성되지 않음)으로 도출된다.
무기 에스테르
에스테르도 무기산에서 유래할 수 있다.
- 인산염은 인산 에스테르(예: 트리페닐인산)를 형성한다.
- 황산은 황산에스테르를 형성한다.예를 들어 디메틸황산염
- 질산은 질산에스테르를 형성한다.예를 들어 질산메틸과 같은
- 붕산은 붕산염(예: 트리메틸붕산염)을 형성한다.
- 탄산염은 탄산 에스테르를 형성한다.예를 들어 탄산 에틸렌
호변이체로 존재하는 무기산은 다양한 에스테르를 형성한다.
- 인산은 트리에틸포스파이트(P(OEt)3와 디에틸포스파이트(HP(O)(OEt))2의 두 가지 종류의 인산에스테르를 형성한다.
불안정하거나 포착하기 어려운 무기산은 안정적인 에스테르를 형성합니다.
- 지금까지 검출된 적이 없는 크롬산은 디옥시리보브틸크롬산염을 형성한다
- 드문 황산은 디메틸설파이트를 형성한다
원칙적으로, 수백 개로 알려진 모든 금속과 금속 알콕시드는 가상의 산의 에스테르로 분류될 수 있다.
구조 및 본딩
에스테르에는 120° C–C–O 및 O–C–O 각도가 발생하는 카르보닐 중심이 포함되어 있습니다.아미드와 달리, 에스터는 C–O–C 결합에 대한 회전이 낮은 장벽을 가지기 때문에 구조적으로 유연한 기능성 기이다.유연성과 저극성은 물리적 특성에 나타나며, 해당 [5]아미드보다 덜 단단하고(낮은 녹는점), 휘발성이 높은(낮은 끓는점) 경향이 있습니다.에스테르에 있는 α-수소의a pK는 약 [6]25이다.
많은 에스테르들은 입체구조 이성질체의 가능성을 가지고 있지만, 과접합과 쌍극자 최소화 효과의 조합으로 인해 s-트랜스(또는 E) 대안보다는 s-cis(또는 Z) 배열을 채택하는 경향이 있다.Z 형태에 대한 선호도는 치환기 및 용매([7][8]존재하는 경우)의 특성에 따라 영향을 받습니다.작은 고리를 가진 락톤은 순환 구조 때문에 s-트랜스(즉, E)로 제한됩니다.
물리적 특성과 특성
에스터는 에테르보다 극성이 높지만 알코올보다는 극성이 낮다.이들은 수소 결합 수용체로 수소 결합에 참여하지만, 부모 알코올과 달리 수소 결합 기증자로서의 역할을 할 수 없습니다.수소 결합에 참여하는 이러한 능력은 약간의 수용성을 부여한다.수소 결합 기증 능력이 부족하기 때문에 에스테르들은 자기 결합을 하지 않는다.따라서 에스터는 분자량이 [5]유사한 카르본산보다 휘발성이 높다.
특성화 및 분석
에스테르는 일반적으로 휘발성을 이용하여 가스 크로마토그래피로 식별된다.에스테르에 대한 IR 스펙트럼은 §에C=O 할당된 1730-1750cm−1 범위의 강렬한 선명한 대역을 특징으로 한다.이 피크는 카르보닐에 부착된 관능기에 따라 달라집니다.예를 들어, 벤젠 고리 또는 카르보닐과 결합하는 이중 결합은 파장을 약 30cm−1 아래로 떨어뜨립니다.
응용 프로그램 및 발생 항목
에스테르는 자연계에서 널리 사용되고 있으며 산업에서도 널리 사용되고 있습니다.자연에서, 지방은 일반적으로 글리세롤과 [10]지방산으로부터 파생된 트리터이다.에스터는 사과, 두리안, 배, 바나나, 파인애플,[11] 딸기를 포함한 많은 과일들의 향을 담당합니다.폴리에틸렌 테레프탈레이트, 아크릴산에스테르, 셀룰로오스 아세테이트 [12]등 매년 수십억 킬로그램의 폴리에스테르가 산업적으로 생산된다.
준비
에스테르화는 두 가지 반응 물질(일반적으로 알코올과 산)이 반응 생성물로 에스테르를 형성하는 화학 반응의 총칭입니다.에스테르는 유기 화학 및 생물학적 물질에 흔히 사용되며, 종종 쾌적하고 과일 냄새가 난다.이것은 향기 및 향미 산업에서 광범위하게 사용되는 것으로 이어진다.에스테르 결합은 또한 많은 폴리머에서 발견된다.
알코올에 의한 카르본산에스테르화
전형적인 합성은 피셔 에스테르화로, 탈수제가 있는 상태에서 카르본산을 알코올로 처리하는 것을 포함합니다.
- RCOH2 + ROH r22 RCOR + + HO
이러한 반응에 대한 평형 상수는 전형적인 에스테르(예: 초산 [13]에틸)의 경우 약 5이다.촉매가 없으면 반응이 느립니다.황산은 이 반응의 대표적인 촉매이다.고분자 술폰산과 같은 다른 많은 산들도 사용된다.에스테르화는 가역성이 높기 때문에 르 샤틀리에의 원리를 사용하여 에스테르 수율을 개선할 수 있습니다.
- 과도한 알코올 사용(용매로 사용)
- 탈수제 사용: 황산은 반응을 촉매할 뿐만 아니라 물(반응 생성물)을 분리한다.분자 체와 같은 다른 건조제들도 효과적이다.
- Dean-Stark 장치와 연계하여 톨루엔과 함께 저비등 공저액으로 증류하는 등의 물리적 수단에 의한 물 제거.
시약은 알코올과 카르본산 혼합물의 탈수를 촉진하는 것으로 알려져 있습니다.예를 들어, Steglich esterification은 가벼운 조건에서 에스테르를 형성하는 방법입니다.이 방법은 펩타이드 합성에 널리 쓰이며, 기질은 높은 열과 같은 가혹한 조건에 민감합니다.카르본산을 활성화하여 더욱 반응시키기 위해 DCC(디시클로헥실카르보디이미드)를 사용하고 아실전달촉매로는 4-디메틸아미노피리딘(DMAP)을 사용한다.[14]
알코올과 카르본산의 혼합물을 탈수하는 또 다른 방법은 미츠노부 반응이다.
- RCOH2 + RΩOH + P(CH65)3 + RN22 → RCOR2 + OP(CH65)3 + RNH222
카르본산은 디아조메탄을 사용하여 에스테르화할 수 있다.
- RCOH2 + CHN22 → RCOCH23 + N2
이 디아조메탄을 사용하면, 예를 들어 가스 크로마토그래피에 의한 분석을 위해 카르본산의 혼합물을 거의 정량적인 수율로 메틸에스테르로 변환할 수 있다.이 방법은 특수 유기 합성 작업에는 유용하지만 대규모 애플리케이션에는 너무 위험하고 비용이 많이 드는 것으로 간주됩니다.
에폭시드에 의한 카르본산에스테르화
카르본산은 에폭시드로 처리하여 β-히드록시스터로 에스테르화된다.
- RCOH2 + RCHCHO2 → RCOCH22(OH)R
이 반응은 아크릴산으로부터 비닐 에스테르 수지 수지 생산에 사용된다.
아실염화물 및 산무수물의 알코홀리시스
알코올은 아실 염화물 및 산성 무수물과 반응하여 에스테르를 생성합니다.
- RCOCl + R'OH → RCOR2 + HCl
- (RCO)2O + R'OH → RCOR2 + RCOH2
이 반응은 되돌릴 수 없는 단순 작업입니다.아실염화물과 산무수물도 물과 반응하므로 무수조건이 바람직하다.아민은 물보다 더 강한 핵 친화력이 있고 반응 속도가 더 빠르기 때문에 아미드를 만들기 위한 아민의 유사 아실화는 덜 민감하다.이 방법은 비용이 많이 들기 때문에 실험실 규모의 시술에만 사용됩니다.
카르본산염의 알킬화
카르복실산 음이온의 염은 에스테르화에 널리 이용되지는 않지만 할로겐화 알킬화제로 [12]에스테르를 만들 수 있다.염화알킬을 사용하는 경우에는 요오드화염이 반응을 촉매할 수 있다(핀켈슈타인 반응).카르본산염은 종종 [15]제 자리에서 생성된다.어려운 경우에는 할로겐화물에 대한 은이온좌표가 이탈을 촉진하고 반응속도를 향상시키므로 카르복실산은을 사용할 수 있다.이 반응은 음이온 가용성 문제로 인해 발생할 수 있으며, 따라서 상전달 촉매 또는 DMF와 같은 극성 비프로틱 용제의 추가에 의해 이점을 얻을 수 있습니다.
에스테르 변환
한 에스테르를 다른 에스테르로 바꾸는 성전환은 널리 행해지고 있습니다.
- RCOR2 + CHOH3 → RCOCH23 + RΩOH
가수분해와 마찬가지로, 트랜스 에스테르화는 산과 염기에 의해 촉매된다.이 반응은 예를 들어 지방산에스테르 및 알코올 생산에서 트리글리세리드 분해에 널리 사용됩니다.폴리(에틸렌 테레프탈레이트)는 디메틸 테레프탈레이트 및 에틸렌 글리콜의 [12]에스테르 교환에 의해 생성됩니다.
- (CH64)(COCH)232 + 2 CH24(OH)2 →1µn {(CH64)(CO224)(2CH)}n + 2 CHOH3
트랜스 에스테르화의 서브셋은 디케틴의 알코홀리시스이다.이 반응은 2개의 케토스터를 [12]제공한다.
- (CHCO2)2 + ROH → CHC3(O)CHCOR22
카르보닐화
알케인은 금속 카르보닐 촉매의 존재 하에서 "히드로에스테르화"된다.프로판산에스테르류는 다음과 같은 방법으로 상업적으로 생산된다.
- CH24 + ROH + CO → CHCOR252
프로피온산메틸의 전제가 하나의 예시이다.
- CH24 + CO + MeOH → MeOCCHH223
메탄올의 카르보닐화는 포름산의 주요 상업적 공급원인 메틸포름산염을 생산한다.반응은 메톡시드 나트륨에 의해 촉매된다.
- CHOH3 + CO → CHOCH32
알켄 및 알킨에 카르본산 첨가
수산화에서 알케인과 알킨은 카르본산의 H-O 결합에 삽입된다.아세트산비닐은 아세틸렌에 아세트산을 첨가하여 [16]공업적으로 생산된다.현재 아세트산아연은 촉매로 사용된다.
- CHCOH32 + CH22 → CHCOCH322
아세트산비닐은 에틸렌, 아세트산 및 산소의 팔라듐 촉매 반응에 의해 생성될 수도 있습니다.
- CH24 + CHCOH32 + 1⁄22 O → CHOCH2323 + HO2
규소퉁스트산은 에틸렌에 의한 아세트산의 알킬화에 의해 아세트산에틸을 제조하는 데 사용된다.
- CH24 + CHCOH32 → CHCOCH3225
알데하이드에서
티쉬첸코 반응은 에스테르를 만들기 위해 무수 염기의 존재 하에서 알데히드의 불균형을 포함한다.촉매는 알루미늄 알콕사이드 또는 나트륨 알콕사이드입니다.벤즈알데히드는 벤질옥시드나트륨(나트륨 및 벤질알코올로부터 생성됨)과 반응하여 [17]벤질벤조산염을 생성합니다.이 방법은 [12]아세트알데히드에서 아세트산에틸을 제조하는 데 사용됩니다.
기타 방법
- 염기가 있는 상태에서 α-할로케톤의 Favoreskii 재배열
- 베이어-빌리거 케톤과 과산화물 산화
- 질소와 알코올의 피너 반응
- 금속-아실 복합체의 친핵성 추상화
- 수산 중의 정형외과 가수분해
- 에스테르화에[18] 의한 셀룰 분해
- 염산과 다양한 [19]알코올이 존재하는 상태에서 워크업을 사용하여 알케인을 오존 분해한다.
- 메틸에스테르로 [20]이어지는 메틸케톤의 양극산화.
- 관심화는 다른 에스테르들의 지방산 그룹을 교환한다.
반응
에스테르는 카보닐 카본에서 친핵체와 반응한다.카르보닐은 약하게 친전자성이지만 강한 친핵성(아민, 알콕시드, 수소화물, 유기석소 화합물 등)의 공격을 받습니다.카르보닐에 인접한 C-H 결합은 약산성이지만 강한 염기로 탈양성된다.이 과정은 보통 응축 반응을 일으키는 과정입니다.에스테르 내 카르보닐 산소는 약염기성이며, 아미드 내 질소의 전자 쌍 공진 기증으로 인해 아미드 내 카르보닐 산소보다 적지만 부가물을 형성한다.
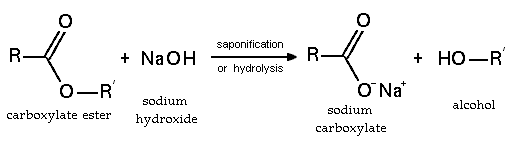
가수분해와 비누화
에스테르화는 가역적인 반응이다.에스테르는 산성 및 염기성 조건에서 가수분해된다.산성 조건 하에서 반응은 피셔 에스테르화의 역반응입니다.기본 조건 하에서 수산화물은 친핵체로 작용하고 알콕시드는 이탈기이다.이 반응, 비누화는 비누 제조의 기본이다.
또한 알콕시드기는 암모니아나 1차 또는 2차 아민과 같은 더 강한 핵 친성에 의해 대체될 수 있습니다. (암모 분해 반응)
- RCOR2 + NHR2 → RCONHR + ROH
이 반응은 보통 되돌릴 수 없다.아민 대신 히드라진과 히드록실아민을 사용할 수 있다.에스테르들은 로센 재배열에서 중간 하이드록사미드산을 통해 이소시아네이트로 전환될 수 있다.
예를 들어 그리냐드 시약과 유기석소 화합물과 같은 탄소 친핵성분의 공급원은 카르보닐에 쉽게 첨가된다.
축소
케톤이나 알데하이드와 비교했을 때 에스테르는 상대적으로 환원성이 강하다.20세기 초에 촉매 수소화의 도입은 획기적인 발전이었다; 지방산의 에스터는 지방 알코올로 수소화된다.
- RCOR2 + + 22 H → RCHOH2 + R oh OH
전형적인 촉매는 구리 크롬산염입니다.촉매 수소화가 개발되기 전에는 Bouveault-Blanc 환원을 사용하여 에스테르를 대규모로 감소시켰다.이 방법은 대부분 구식이지만 양성자 선원의 존재 하에서 나트륨을 사용한다.
특히 미세 화학 합성에서는 리튬 수소화 알루미늄을 사용하여 에스테르를 2개의 1차 알코올로 환원합니다.관련 시약인 붕화수소나트륨은 이 반응이 느립니다.DIBAH는 에스테르를 알데히드로 [21]환원한다.
중간 헤미아세탈은 분해되어 알코올과 알데히드(급감하여 제2의 알코올을 얻을 수 있음)를 생성하는 경향이 있기 때문에 해당 에테르를 직접 환원하는 것은 어렵다.반응은 다양한 [22][23]Lewis산과 함께 트리에틸실란을 사용하여 달성할 수 있습니다.
알데히드는 에스테르 중 카르복실기와 인접한 탄소상의 수소원자가 탈양성자화(α to)를 하기에 충분한 산성으로 다양한 유용한 반응을 일으킨다.탈양성자화에는 알콕시드와 같은 비교적 강한 염기가 필요합니다.탈양성자는 예를 들어 클라이젠 응축과 분자 내 등가물인 디크만 응축과 같은 추가적인 반응을 일으킬 수 있는 친핵성 에놀라트를 제공한다.이 변환은 말론산의 다이에스터가 전자 친필(예를 들어 할로겐화 알킬)과 반응하는 말론 에스테르 합성에 이용되며, 이후 탈탄산된다.또 다른 변형으로는 Fratter-Seebach 알킬화가 있다.
기타 반응
- 페닐에스테르들은 감자튀김 재배열에서 히드록시아릴케톤에 반응한다.
- Chan 전위에서는 특정 에스테르를 α-히드록실기로 기능화한다.
- β수소 원자를 가진 에스테르를 에스테르 열분해 시 알케인으로 변환할 수 있다.
- 에스테르를 [24]질화물로 직접 변환합니다.
그룹 보호
에스테르류는 카르본산을 보호하는 역할을 한다.카르본산 보호는 펩타이드 합성에 유용하여 2관능성 아미노산의 자가반응을 방지한다.메틸과 에틸에스테르는 일반적으로 많은 아미노산에 사용 가능하다; t-부틸에스테르는 더 비싼 경향이 있다.단, t-부틸에스테르는 강산성 조건 하에서 카르본산 및 이소부틸렌을 얻기 위해 제거되기 때문에 특히 유용하다.
에스테르 향기제 목록
많은 에스테르들은 독특한 과일 같은 냄새를 가지고 있으며, 많은 에스테르들은 식물의 에센셜 오일에서 자연적으로 발생한다.이것은 또한 그러한 냄새를 모방하는 것을 목적으로 하는 인공 향료나 향수에 널리 쓰이게 되었다.
| 에스터명 | 구조. | 냄새 또는 발생 |
|---|---|---|
| 육산알릴 | 파인애플. | |
| 아세트산벤질 | 배, 딸기, 재스민 | |
| 아세트산 보닐 |  | 소나무 |
| 아세트산 부틸 | 사과, 여보 | |
| 부틸낙산염 | 파인애플. | |
| 프로판산 부틸 | 배방울 | |
| 아세트산에틸 | 매니큐어 리무버, 모형 페인트, 모형 비행기 접착제, 배 | |
| 안식향산에틸 | 스위트, 윈터그린, 프루티, 메디컬, 체리, 포도 | |
| 낙산에틸 | 바나나, 파인애플, 딸기 | |
| 에틸헥사노에이트 | 파인애플, 왁시그린 바나나 | |
| 계피산에틸 | 계피 | |
| 포름산 에틸 | 레몬, 럼, 딸기 | |
| 에틸헵탄산염 | 살구, 체리, 포도, 산딸기 | |
| 이소발산에틸 | 사과 | |
| 젖산 에틸 |  | 버터, 크림 |
| 에틸노에이트 | 포도 | |
| 펜탄산 에틸 | 사과 | |
| 아세트산 게라닐 | 제라늄 | |
| 낙산게라닐 | 체리 | |
| 펜탄산 게라닐 | 사과 | |
| 아세트산 이소부틸 |  | 체리, 산딸기, 딸기 |
| 포름산 이소부틸 | 라즈베리 | |
| 아세트산 이소아밀 | 배, 바나나(배방울로 향미) | |
| 아세트산 이소프로필 | 프루티 | |
| 아세트산 리날릴 | 라벤더, 세이지 | |
| 부틸산리날릴 | 복숭아색 | |
| 포름산리날릴 | 사과, 복숭아 | |
| 아세트산메틸 |  | 딱풀 |
| 안트라닐산메틸 |  | 포도, 재스민 |
| 안식향산메틸 |  | 프루티, 일랑일랑, 페이조아 |
| 부탄산메틸(부탄산메틸) | 파인애플, 사과, 딸기 | |
| 계피산메틸 | 딸기 | |
| 펜탄산메틸(메틸발산메틸) | 꽃다운 | |
| 메틸페닐아세테이트 | 꿀 | |
| 살리실산메틸(윈터그린 오일) |  | 현대적인 루트 맥주, wintergreen, Germolene 및 Ralgex 연고(영국) |
| 카프릴산 노닐 | 오렌지색 | |
| 초산옥틸 | 프루티한 맛의 | |
| 옥틸낙산염 | 스니프 | |
| 아세트산아밀(아세테이트펜틸) | 사과, 바나나 | |
| 낙산펜틸(낙산아밀) | 살구, 배, 파인애플 | |
| 헥사노산펜틸(아밀 카프로에이트) | 사과, 파인애플 | |
| 펜탄산펜틸(아밀발라트) | 사과 | |
| 아세트산프로필 | 먹는 배 | |
| 프로필헥사노에이트 | 블랙베리, 파인애플, 치즈, 와인 | |
| 프로필 이소낙산염 | 럼주 | |
| 테르페닐낙산염 |  | 체리 |
「 」를 참조해 주세요.
- 에스테르 목록
- 산소가 질소로 대체된 에스테르 유사물인 아미드
- 시안산에스테르
- 올리고에스테르
- 폴리올에스테르
- 티오에스테르, 산소를 유황으로 대체한 에스테르 유사물
- 에스테르 변환
- 에테르 지질
레퍼런스
- ^ IUPAC, 화학 용어집, 제2판('골드북') (1997).온라인 수정판: (2006–) "에스터" . doi : 10.1351 / goldbook . E02219
- ^ Cameron Wright (1986). A worker's guide to solvent hazards. The Group. p. 48. ISBN 9780969054542.
- ^ E. Richard Booser (21 December 1993). CRC Handbook of Lubrication and Tribology, Volume III: Monitoring, Materials, Synthetic Lubricants, and Applications. CRC. p. 237. ISBN 978-1-4200-5045-5.
- ^ Leopold Gmelin, Handbuch der Chemie, 제4권: Handbuch der Organischen Chemie (제1권) (하이델베르크, 바덴(독일):Karl Winter, 1848), 182쪽.
원문:
번역:b. Ester oder sauerstoffsaeure Aetherarten.
Ethers du troisiéme 장르.
Vielle mineralische und Sauerstoffséuren treiner Alkohol-Art unter Ausscheidung von Wasser zu nutralen fluchitigen äisisisisisisisisisis alsis als als als g g g als als als als als als als als als als als als als als als als als als als als als als als als als als als als als als alsb. 에스테르 또는 옥시산 에테르
세 번째 타입의 에테르
산소를 포함한 많은 미네랄 및 유기산은 물을 제거하면 알코올과 결합하여 중성 휘발성 에테르 화합물 또는 라디칼 이론에 따르면 산이 에테르와 결합하는 소금으로 볼 수 있습니다. - ^ a b J. Advanced Organic Chemistry 4th Ed. J. Wiley and Sons, 1992년 3월:뉴욕.ISBN 0-471-60180-2.
- ^ "Chemistry of Enols and Enolates – Acidity of alpha-hydrogens".
- ^ Diwakar M. Pawar; Abdelnaser A. Khalil; Denise R. Hooks; Kenneth Collins; Tijuana Elliott; Jefforey Stafford; Lucille Smith; Eric A. Noe (1998). "E and Z Conformations of Esters, Thiol Esters, and Amides". J. Am. Chem. Soc. 120 (9): 2108–2112. doi:10.1021/ja9723848.
- ^ Christophe Dugave; Luc Demange (2003). "Cis−Trans Isomerization of Organic Molecules and Biomolecules: Implications and Applications". Chem. Rev. 103 (7): 2475–2932. doi:10.1021/cr0104375. PMID 12848578.
- ^ A. A. Yakovenko, J. H. Gallegos, M. Yu. Antipin, A. Masunov, T. V. Timofeeva (2011). "Crystal Morphology as an Evidence of Supramolecular Organization in Adducts of 1,2-Bis(chloromercurio)tetrafluorobenzene with Organic Esters". Cryst. Growth Des. 11 (9): 3964–3978. doi:10.1021/cg200547k.