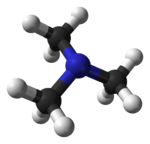
Trimetilamina
| Trimetilamina[1] | |
|---|---|
 | |
|

|
PIN: N,N-Dimetilmetanamina | |
Outros nomes (Trimetil)amina (en realidade, o nome trimetilamina está desaconsellado)[2] | |
| Identificadores | |
| Número CAS | 75-50-3 |
| PubChem | 1146 |
| ChemSpider | 1114 |
| UNII | LHH7G8O305 |
| Número CE | 200-875-0 |
| Número UN | 1083 |
| KEGG | C00565 |
| ChEBI | CHEBI:18139 |
| ChEMBL | CHEMBL439723 |
| Número RTECS | PA0350000 |
| Referencia Beilstein | 956566 |
| 3DMet | B00133 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C3H9N |
| Masa molar | 59,11 g mol−1 |
| Aspecto | Gas incoloro |
| Olor | a peixe e amoniacal |
| Densidade | 670 kg m−3 (a 0 °C) 627,0 kg m−3 (a 25 °C) |
| Punto de fusión | 15 322 °C; 27 611 °F; 15 595 K |
| Punto de ebulición | 3–7 °C; 37–44 °F; 276–280 K |
| Solubilidade en auga | Miscible |
| log P | 0,119 |
| Presión de vapor | 188,7 kPa (a 20 °C)[3] |
| kH | 95 μmol Pa−1 kg−1 |
| Basicidade (pKb) | 4,19 |
| Momento dipolar | 0,612 D |
| Termoquímica | |
| Entalpía estándar de formación ΔfH |
−24,5 to −23,0 kJ mol−1 |
| Perigosidade | |
| Pictogramas GHS | 
|
| Palabra sinal GHS | DANGER |
| declaración de perigosidade GHS | 220 , 315 , 318 , 332 , 335 |
| declaración de precaución GHS | 210 , 261 , 280 , 305+351+338 |
| NFPA 704 | |
| Punto de inflamabilidade | −7 °C; 19 °F; 266 K |
| Límites de explosividade | 2–11.6% |
| LD50 | 500 mg kg−1 (oral, rata) |
| Compostos relacionados | |
| aminas relacionados | Dimetilamina, N-nitrosodimetilamina, dietilamina, trietilamina, diisopropilamina, dimetilaminopropilamina, dietilenetriamina, N,N-diisopropiletilamina, triisopropilamina, tris(2-aminoetil)amina, mecloretamina, HN1 (mostaza nitroxenada) |
| Compostos relacionados | Dimetilhidrazina asimétrica, biguanida, ditiobiuret |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A trimetilamina (TMA) ou N,N-dimetilmetanamina é un composto orgánico coa fórmula N(CH3)3. É unha amina terciaria incolora, higroscópica e inflamable. É un gas a temperatura moderada pero véndese habitualmente en forma de solución en auga ao 40%, pero tamén se vende presurizada en bombonas de gas. A TMA é unha base nitroxenada e pode ser doadamente protonada para dar lugar ao catión trimetilamonio. O cloruro de trimetilamonio é un sólido incoloro higroscópico preparado a partir de ácido clorhídrico. A trimetilamina é un bo nucleófilo e nesta reacción baséanse a maioría das suas aplicacións. A TMA é amplamente utilizada na industria: úsase na síntese de colina, hidróxido de tetrametilammonio, reguladores do crecemento de plantas ou herbicidas, resinas de intercambio iónico moi básicas, axentes de nivelación de tinturas e outras tinturas básicas.[4][5] A altas concentracións ten un cheiro similar ao do amoníaco e pode causar a necrose das membranas mucosass por contacto.[6] A concentracións baixas ten un cheiro a peixe, o cheiro asociado co peixe en descomposición.
En humanos a inxestión de certos alimentos vexetais e animais (por exemplo carne vermella, xema de ovo) que conteñen lecitina, colina e L-carnitina proporciona a certas especies da flora intestinal os substratos para sintetizar TMA, a cal é despois absorbida no torrente sanguíneo.[7][8] Os niveis altos de trimetilamina no corpo están asociados co desenvolvemento da trimetilaminuria (ou síndrome do cheiro a peixe), causada por un defecto xenético no encima que degrada a TMA ou por tomar grandes doses de suplementos que conteñen colina ou L-carnitina.[7][8] A TMA é metabolizada polo fígado a N-óxido de trimetilamina (TMAO). O TMAO está sendo investigado como unha posible substancia proateroxénica que pode acelerar a aterosclerose naqueles que comen alimentos cun alto contido en precursores da TMA.[8] A TMA tamén causa o cheiro dalgunhas infeccións humanas, o mal alento e a vaxinose bacteriana.
A trimetilamina é un agonista completo do TAAR5 humano,[9][10][11] un receptor asociado a aminas traza que se expresa no epitelio olfactorio e funciona como un receptor olfactorio para aminas terciarias.[11][12] Un ou máis receptores de olores adicionais tamén parecen estar implicados na olfacción da trimetilamina en humanos.[12]
Produción
[editar | editar a fonte]A trimetilamina prepárase por medio da reacción entre o amoníaco e o metanol empregando un catalizador:[4]
- 3 CH3OH + NH3 → (CH3)3N + 3 H2O
Esta reacción coproduce as outras metilaminas, dimetilamina (CH3)2NH e metilamina CH3NH2.
A trimetilamina tamén foi preparada por medio dunha reacción entre o cloruro de amonio e o paraformaldehido:[13]
- 9 (CH2=O)n + 2n NH4Cl → 2n (CH3)3N•HCl + 3n H2O + 3n CO2↑
Toxicidade
[editar | editar a fonte]Os efectos agudo e crónico da TMA xa se sinalaron na literatura médica no século XIX. A TMA causa irritación ocular e cutánea e suxeriuse que é unha toxina urémica.[14] En pacientes, a trimetilamina causa dor de estómago, vómitos, diarrea, lacrimación, agrisamento da pel e axitación.[15] Ademais diso, tamén se informou de toxicidade reprodutiva/no desenvolvemento.[6]
Dispóñense de directrices que sinalan límites de exposición para traballadores, por exemplo a Recomendación do Comité Científico sobre Límites de Exposición Laboral da Comisión da Unión Europea.[16]
Algúns estudos experimentais suxiren que a TMA pode estar implicada na etioloxía das doenzas cardiovascularess.[17][18]
Aplicacións
[editar | editar a fonte]A trimetilamina utilízase na síntese da colina, hidróxido de tetrametilammonio, reguladores do crecemento de plantas, herbicidas, resinas de intercambio iónico moi básicas, axentes niveladores de tinturas e diversas tinturas básicas.[4][5] Os sensores de gas para detectar a frescura dos peixes detectan a trimetilamina.
Reaccións
[editar | editar a fonte]A trimetilamina é unha base de Lewis que forma adutos con diversos ácidos de Lewis.[19]
Trimetilaminuria
[editar | editar a fonte]A trimetilaminuria é un trastorno xenético autosómico recesivo que implica un defecto na función ou expresión da monooxixenase que contén flavina 3 (FMO3) que orixina un metabolismo da trimetilamina alterado. As persoas que padecen trimetilaminuria desenvolven un característico cheiro a peixe (o cheiro da trimetilamina) na súa suor, urina e alento despois de inxerir alimentos ricos en colina. Unha condición similar á trimetilaminuria observouse tamén nunha certa raza de polos chamada Rhode Island Red que produce ovos con cheiro a peixe, especialmente despois de que os animais coman alimentos que conteñen unha alta proporción de colza.[20][21]
Notas
[editar | editar a fonte]- ↑ Merck Index, 11ª edición, 9625.
- ↑ IUPAC Chemical Nomenclature and Structure Representation Division (2013). "P-62.2.2.1". En Favre, Henri A.; Powell, Warren H. Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. IUPAC–RSC. ISBN 978-0-85404-182-4.
- ↑ Swift, Elijah; Hochanadel, Helen Phillips (maio de 1945). "The Vapor Pressure of Trimethylamine from 0 to 40°". Journal of the American Chemical Society 67 (5): 880–881. doi:10.1021/ja01221a508.
- ↑ 4,0 4,1 4,2 Van Gysel, August B.; Musin, Willy (2000). "Methylamines". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a16_535.
- ↑ 5,0 5,1 Ashford, Robert D. (2011). Ashford's Dictionary of Industrial Chemicals (3rd ed.). p. 9362. ISBN 978-0-9522674-3-0.
- ↑ 6,0 6,1 "Trimethylamine [MAK Value Documentation, 1983]". The MAK-Collection for Occupational Health and Safety. Wiley-VCH Verlag GmbH & Co. KGaA. 2014-10-27. pp. 1–9. ISBN 978-3527600410. doi:10.1002/3527600418.mb7550e0914.
- ↑ 7,0 7,1 Falony G, Vieira-Silva S, Raes J (2015). "Microbiology Meets Big Data: The Case of Gut Microbiota-Derived Trimethylamine". Annu. Rev. Microbiol. 69: 305–321. PMID 26274026. doi:10.1146/annurev-micro-091014-104422.
revisamos a literatura sobre a trimetilamina (TMA), un metabolito xerado pola microbiota ligado ao desenvolvemento da ateriosclerose.
- ↑ 8,0 8,1 8,2 Gaci N, Borrel G, Tottey W, O'Toole PW, Brugère JF (novembro de 2014). "Archaea and the human gut: new beginning of an old story". World J. Gastroenterol. 20 (43): 16062–16078. PMC 4239492. PMID 25473158. doi:10.3748/wjg.v20.i43.16062.
A trimetilamina é exclusivamente un produto derivado da microbiota de nutrientes (lecitina, colina, TMAO, L-carnitina) procedentes da dieta normal, a partir dos cales parecen orixinarse dúas doenzas: trimetilaminuria (ou síndrome do cheiro a peixe) e doenza cardiovascular por medio da propiedade proateroxénica da súa forma oxidada derivada do fígado.
- ↑ Wallrabenstein I, Kuklan J, Weber L, Zborala S, Werner M, Altmüller J, Becker C, Schmidt A, Hatt H, Hummel T, Gisselmann G (2013). "Human trace amine-associated receptor TAAR5 can be activated by trimethylamine". PLOS ONE 8 (2): e54950. Bibcode:2013PLoSO...854950W. PMC 3564852. PMID 23393561. doi:10.1371/journal.pone.0054950.
- ↑ Zhang J, Pacifico R, Cawley D, Feinstein P, Bozza T (febreiro 2013). "Ultrasensitive detection of amines by a trace amine-associated receptor". J. Neurosci. 33 (7): 3228–39. PMC 3711460. PMID 23407976. doi:10.1523/JNEUROSCI.4299-12.2013.
Demostramos que o [TAAR5 humano] responde á amina terciaria N,N-dimetiletilamina e en menor medida á trimetilamina, un agonista estruturalmente relacionado do TAARS de ratos e ratas (Liberles and Buck, 2006; Staubert et al., 2010; Ferrero et al., 2012).
- ↑ 11,0 11,1 Zhang LS, Davies SS (abril del 2016). "Microbial metabolism of dietary components to bioactive metabolites: opportunities for new therapeutic interventions". Genome Med 8 (1): 46. PMC 4840492. PMID 27102537. doi:10.1186/s13073-016-0296-x.
Táboa 2: Microbial metabolites: their synthesis, mechanisms of action, and effects on health and disease
Figura 1: Molecular mechanisms of action of indole and its metabolites on host physiology and disease - ↑ 12,0 12,1 Liberles SD (outubro de 2015). "Trace amine-associated receptors: ligands, neural circuits, and behaviors". Curr. Opin. Neurobiol. 34: 1–7. PMC 4508243. PMID 25616211. doi:10.1016/j.conb.2015.01.001.
- ↑ Adams, Roger; Marvel, C. S. (1921). "Trimethylamine Hydrochloride". Organic Syntheses 1: 79. doi:10.15227/orgsyn.001.0079.
- ↑ Wills, M. R.; Savory, J. (1981). "Biochemistry of renal failure". Annals of Clinical and Laboratory Science 11 (4): 292–9. PMID 7023344.
- ↑ "Gifte und Vergiftungen. Vierte Ausgabe des Lehrbuches der Toxikologie. Von Prof. Louis Lewin. Mit 41 Figuren und einer farbigen Spektraltafel. Berlin 1929. Verlag von Georg Stilke. 1087 Seiten. Preis geh. 50,— Mark, geb. 55,— Mark". Archiv der Pharmazie 267 (4): 322–323. 1929. ISSN 0365-6233. doi:10.1002/ardp.19292670410.
- ↑ European Commission. Directorate-General for Employment, Social Affairs and Inclusion. Scientific Committee on Occupational Exposure Limits. (2017). SCOEL/REC/179 trimethylamine recommendation from the Scientific Committee on Occupational Exposure Limits. Publications Office. OCLC 1032584642.
- ↑ Jaworska, Kinga; Bielinska, Klaudia; Gawrys-Kopczynska, Marta; Ufnal, Marcin (2019-08-27). "TMA (trimethylamine), but not its oxide TMAO (trimethylamine-oxide), exerts hemodynamic effects - implications for interpretation of cardiovascular actions of gut microbiome.". Cardiovascular Research 115 (14): 1948–1949. ISSN 0008-6363. PMID 31504256. doi:10.1093/cvr/cvz231.
- ↑ Jaworska, Kinga; Hering, Dagmara; Mosieniak, Grażyna; Bielak-Zmijewska, Anna; Pilz, Marta; Konwerski, Michał; Gasecka, Aleksandra; Kapłon-Cieślicka, Agnieszka; Filipiak, Krzysztof (2019-08-26). "TMA, A Forgotten Uremic Toxin, but Not TMAO, Is Involved in Cardiovascular Pathology". Toxins 11 (9): 490. ISSN 2072-6651. PMC 6784008. PMID 31454905. doi:10.3390/toxins11090490.
- ↑ Cramer, R. E.; Bopp, T. T. (1977). "Graphical display of the enthalpies of adduct formation for Lewis acids and bases". Journal of Chemical Education 54: 612–613. doi:10.1021/ed054p612.
- ↑ Pearson, Arthur W.; Butler, Edward J.; Curtis, R. Frank; Fenwick, G. Roger; Hobson-Frohock, Anthony; Land, Derek G. (1979). "Effect of rapeseed meal on trimethylamine metabolism in the domestic fowl in relation to egg taint". Journal of the Science of Food and Agriculture 30 (8): 799–804. doi:10.1002/jsfa.2740300809.
- ↑ Lichovníková, M.; Zeman, L.; Jandásek, J. (2008). "The effect of feeding untreated rapeseed and iodine supplement on egg quality" (PDF). Czech Journal of Animal Science 53 (2): 77–82. doi:10.17221/330-CJAS. Consultado o 19 de decembro de 2016.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]- Amoníaco, NH3
- Amonio, NH4+
- Metilamina, (CH3)NH2
- Dimetilamina
- Trietilamina (TEA)
Ligazóns externas
[editar | editar a fonte]| Wikimedia Commons ten máis contidos multimedia na categoría: Trimetilamina |


